فلوسيتومتری يک تكنولوژی بيوفيزيک بر اساس ليزر است كه برای جدا سازی ، شمارش سلول ، تشخيص بيوماركر و مهندسی پروتئين با عبوردادن سلول ها به صورت تکتک از مقابل ليزر استفاده میشود. اين دستگاه ، امكان آناليز چندپارامتری همزمان مشخصههای شيميايی و يا فيزيكی را تا هزاران ذره در هر ثانيه فراهم میكند.

هدف
فـلـوسـيـتـومـتـری بـه سرعت ، چندين جزء از سـلــول را بــه صــورت هـمــزمــان كـمــی كـرده و سلولها و اجزای آنها را در حالت محلول (به عـنـــوان مـثــال در خــون ، شـسـتـشــوی مـثــانــه ، يــا ديگـر مايعات بدن) میشمارد -يا در برخی از مـوارد از هـم جـدا مـیكند- . كاربردهای بالينی فـلــوسـيـتــومتـرهـا شـامـل تشخيـص و شمـارش زيـرمـجـمـوعـههای لنفوسيت T انسان و انجام شـمـارشهای افتراقی سلولهای سفيد خون ، مـطـالـعـات اتوآنتی بادی پلاكت ، آناليز نشانگر سـطــح سـلــول ، آنـالـيـز رتـيـكـولـوسـيـت و آنـالـيـز بــاكـتــريــايــی اســت. فـلــوسـيـتــومـتـرهـا همچنيـن آنيوپلوئيدی (هر گونه انحرافی از مضرب دقيقی از تعداد هاپلوئيد كروموزوم ها ، چه كمتر و چه بيشتر) را با اندازه گيری داخل سلولی و آناليز DNA ، تشخيص میدهند.
پزشكان ميتوانند از نتايج اين مطالعات در كنار دادههای بالينی ديگر برای تشخيص و پيش بـيـنـی لـوسـمـی ، لـنـفوم ، اختلالات نقص ايمنی مـانـنـد عـفـونت HIV ، بيماریهای خودايمنی و نــاهـنـجــاریهــای جـنـيـنـی و نـيـز بـرای ارزيـابـی مــوفـقـيــت فــرايـنــدهــای پـيــونــد اسـتـفــاده كـننـد. دادههای فلوسيتومتری همچنين در تحقيقات ســـرطـــانـــی بــرای انــدازهگـيــری تـكـثـيــر ، انـجــام ســنــجــــشهــــای انــكــــوپــــروتــئــيــــن و ارزيـــابـــی مـقـــاومـــتهـــای داروئـــی اسـتـفــاده مــیشــونــد. فلوسيتومتری به صورت معمول در تشخيص اخـتـــلالات ، بـــه ويــژه ســرطــان خــون اسـتـفــاده مـــیشـــود ؛ امـــا كـــاربـــردهـــای زيــاد ديـگــری در تحقيقـات پايه ، عمل بالينی و آزمايشات بالينی هم دارد. يک كاربرد معمول آن مرتب كردن فيزيكی ذرات بر اساس خواص آنها است به نحوی كه جمعيت موردنظر خالصسازی شود.
تاريخچه
مختـرع اولين نمونههای فلوسيتومترهای امروزه به ويژه جدا كنندههای سلول ، Mack Fulwyler بود. وی مقاله مرتبط با اين موضوع را در 1965 منتشر كرد. اولين دستگاه فلوسيتومتر بر اساس فلورسنس در 1968 توسط Wolfgang Gohde از دانشگاه مونستر توسعه يافت. در آن زمان ، دانشمندان روشهای جذبی را به روشهای فلورسنس ترجيح میدادند. خيلی طول نكشيد كه دستگاههای فلوسيتومتر شامل سيتوفلوگراف توسعه يافتند.
عنوان فناوری
اسم اصلی فناوری فلوسيتومتر ، "سيتوفتومتری پالس" بود. در پنجمين كنفرانس بنياد مهندسی امريكا روی سيتولوژی اتوماتيک در فلوريدا در 1976 توافق شد كه همه از اسم فلوسيتومتر استفاده كنند و اين نام به سرعت مرسوم شد.
اصول عملكرد
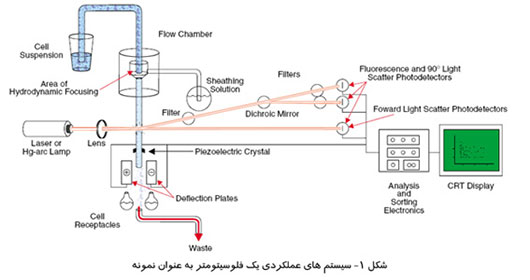
فلوسيتومتری شامل سه سيستم پايه است: جزء مايع كه سلولها را به محفظه آناليز منتقل میكند ، سيستم نوری با وسايل تشخيص و آناليز داده و اجزای نمايشگر (شكل 1) يک پرتو نوری تک طول موج (معمولا نور ليزر) ، به سمت يک جريان مايع متمركز شده به صورت هيدروديناميک هدايت میشود. تعدادی آشكارساز پس از نقطه برخورد جريان مايع با ليزر قرار دارند: يكی در امتداد شعاع نوری (پراكنده كننده فروارد forward scatter يا FSC) و چند تا عمود بر آن (پراكنده كننده جانبی side scatter يا SSC) و يک يا چند آشكارساز فلورسنس. هر ذره معلق با اندازه 0/2 تا 150 ميكرومتر كه از شعاع نور عبور میكند ، نور ليزر را پراكنده می كند. مواد شيميايی فلورسنت موجود در ذره يا متصل شده به آن ، میتوانند تحريک شده و نوری با طول موج بيشتر از منبع نوری ساطع كنند. اين تركيب از نور فلورسنت و نور پراكنده شده ، توسط آشكارسازها و با تحليل نوسانات (يكی برای هر پيک انتشار فلورسنت) تشخيص داده میشود و سپس میتوان انواع مختلفی از اطلاعات در مورد ساختار فيزيكي و شيميايي هر ذره مجزا را استخراج كرد. FSC با حجم سلول همبسته است و SSC وابسته به پيچيدگي داخلی ذره (يعنی شكل هسته ، مقدار و نوع دانه ها در سيتوپلاسم يا زبری غشا) است. چرا كه نور در اثر برخورد با اجزای داخلی سلول پراكنده میشود. برخی از فلوسيتومترهای موجود در بازار ، نياز به فلورسنس ندارند و تنها از پراكنده كنندههای نور برای اندازه گيری استفاده می كنند. بيشتر فلوسيتومترها ، تصاويری از فلورسنس هر سلول ، نور پراكنده شده و نور منتقل شده تشكيل میدهند.
ايمنوفلورسنس پايه اغلب سنجشهای سيتومتريک فلو است. اين تكنيک متكی بر اسـتـفــاده از رنـگهـا و فلئـوروكـرومهـا (flurochromes) بـرای نشـانـه گـذاری كـردن ساختارهای خاص بر روی سلول است. فلئوروكروم به اجزای خاصی در سلول مانند DNA ، RNA يا پروتئينها (آنزيمهای سلولی ، نشانگرهای سطح غشا ، ديگر آنتی ژن ها) متصل می شود. زمانی كه در معرض نوری با طول موج خاص قرار میگيرند ، اين فلئوروكرومها ، فلورسنت میشوند و نور را با طول موج بيشتر از نور تابشی كه جذب میكنند ، ساطع خواهند كرد.
دو يـا چـند فلئوروكروم میتوانند به صورت همزمان برای برچسب گذاری دو تركيب سلولی (به عنوان مثال يكی برای برچسب گذاری DNA هسته و ديگری برای برچسب گذاری آنزيمهای سيتوپلاسمی) استفاده شوند. به علاوه چند فلئوروكروم میتوانند برای برچسب گذاری ماده سلولی مشابهی استفاده شوند. اجزای سلولی میتوانند هم چنين با رنگ ametachromatic برچسب گذاری شوند.
سلولهايی كه قرار است آناليز شوند با معرفهای خاصی تركيب شده و سپس به صورت اتوماتيک در يک جريان مايع معلق میشوند. اين جريان در يک محيط مايع تـحـت فـشـار بـه مـحـفـظـه آنـالـيـز مـنـتـقـل میشود. قبل از ورود به محفظه ، به صورت هـيـدروديـنـامـيک متمركز شده و يک جريان لايه ای و آرام ايجاد می كند. اين باعث میشود كه سلولها به يک مسير دقيقاً تک سلولی از ناحيه سنجش نوری عبور كنند. در اين ناحيه ، سيستم تشخيص ، هر سلول را با نرخ شمارش تا 10 هزار سلول در ثانيه آناليز میكند.
همين طور كه سلولها از محفظه آناليز (فلوسل) عبور می كنند ، يک پرتو نوری تک رنگ با چگالی بالا از يک ليزر به آنها تابانده میشوند. طول موج تابيده شده توسط ليزر بايد در بازه انرژی تحريكی رنگ/فلئوروكرومهای انتخابی قرار بگيرد تا فلورسنت رخ دهد. مرسوم ترين ليزرها ، ليزرهای آرگون هستند كه يک تابش قوی در طول موج nm488 میكنند. هليم-نئون (nm 633) ، هليم-كاديم (nm 325) و ديود قرمز (nm 635) انواع ديگری از ليزرها هستند كه معمولا در فلوسيتومتری استفاده میشوند.
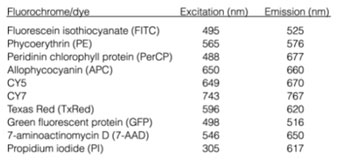
علاوه بر انطباق انرژی ، مهم است كه طول موج تابيده شده توسط ليزر از طول موج انـرژی فـلـورسـانـس قـابل تميز باشد. (جدول 1 را برای مشاهده ليستی از رنگها و fluorochromهای مرسوم ببينيد.)
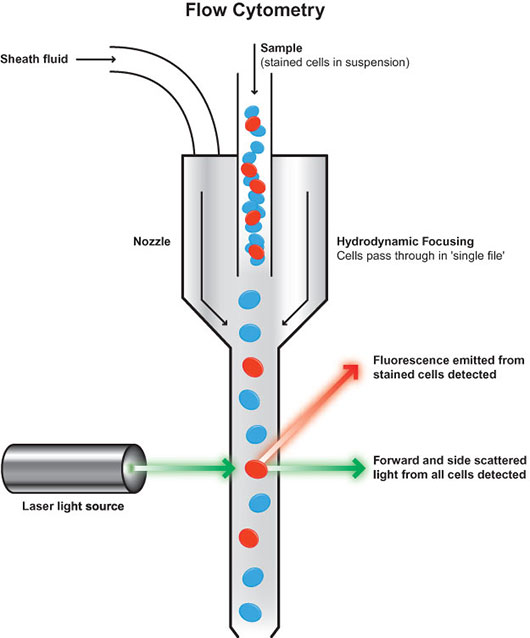
هـمـيـن طـور كـه نـور از داخـل جـريـان سـلـولهـا میگذرد ، دستگاه ، فلورسنس و پراكندگی نوری را كه تابيده ميشود اندازه گيری می كند. پراكندگی نور معياری از مقدار نور ليزر منعكس شده و شكسته شده از طريق سلول در مقايسه با نور منتشر شده از رنگهای فلورسنت است. شدت پراكندگی نور در جهت مقابل (fSc) معمولا متناسب با سايز سلول است ؛ در حالی كه پراكندگی نور در زاويه عمود به نور تابيده شده ، معمولا با ساختارهای داخلی سلول (به عنوان مثال نسبت هسته به سيتوپلاسم ، دانه دانه بودن سيتوپلاسم) مرتبط است. پراكندگی نور میتواند برای تفكيک سلولهای زنده از مرده در يک جمعيت همگن از لنفوسيتها استفاده شود.
مجموعه نور فلورسنت ساطع شده از رشته نمونه معمولا در زاويه 90 درجه نسبت به باريكه نور تابيده شده قرار دارد. تشخيص فلورسانس بر اساس اختصاصی بودن يک رنـگ فـلوورسنت به قسمت منحصربه فردی از سلول است. اين تعامل به تحليل و جـداسـازی زيـرجـمـعـيـتهـای لـنـفـوسـيـت ، انـدازه گـيـری زيـرمجموعه ای از جمعيت لنفوسيتهای T ، ارزيابی كينتيک سلولی در جمعيتهای سلولی نئوپلاستيک و طبيعی ، انـــدازه گـيـــری آنـتـــيژنهـــای سـطـحـــی سـلــول (نشـانگـرهای تومور ، گيرنده ها) ، و جداسازی سلـولهـا بر اساس مشخصههای غشای آنها كمک میكند.
فـلــوسـيـتــومـتــرهــای چـنــد لـيـزری در آنـاليـز سيگنالهای فلورسانسی كه از لحاظ طول موج تحريک جدا از هم هستند ، استفاده می شوند. در اين حالت ، می توان سيگنالهای جداگانه را با استفاده از نيمه آينهها در جهات مختلف هدايت و ارسال كرد ، به نحوی كه هيچ تداخل سيگنالی رخ ندهد. با اين حال در برخی دستگاهها زمانی كـه نور سلول را ترک میكند ، تمام سيگنالها تركيب میشوند. اين متكی به چيدمان آينههای دورنگ نما (dichroic) و فيلترهای جداسازی و اصلاح سيگنالها است. آينههای دورنگنما بـرای منعكس كردن نور بالای يک طول موج خــاص و در عـيــن حــال ردكــردن نـور بـا طـول موجهای پايين تر از آن حد ، طراحی شدهاند. مــیتـوان هميـن طـور كـه نـور وارد لامـپهـای تقويتكننده نوری (pmt) میشود ، فيلتر كردن بيشتری را هم اعمال كرد. اين آشكارسازهای pmt نــور ســاطــع شـده تـوسـط سـلـولهـا را بـه پالسهای الكترونيكی تبديل میكنند و سپس اين پالسها برای ديجيتال شدن و تحليلهای كامپيوتری ، تقويت میشوند.
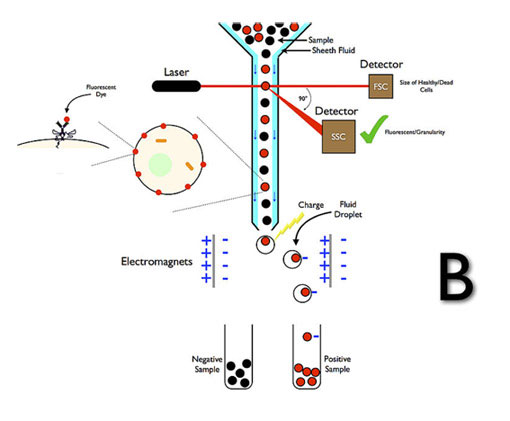
بـرخـی از فلوسيتومترها ، قابليت جداسازی سلول (Sorting) را دارند و میتوانند انواع خاصی از سلولها در نمونه را جداسازی و تحليل كنند. هــمزمــان بــا خــروج رشـتــه نـمــونــه از مـحـفظـه تــشــخــيـــص ، يـــک كـــريــســتــال پـيــزوالـكـتــريــک (كريستالی كه در آن ، نيروی مكانيكی متناسب با ولتاژ اعمال شده توليد میشود) ، ارتعاش كرده و جـريـان يـكـنواخت نمونه را به يک سری قطره تبديل می كند كه از بين دو صفحه انحراف قطبی شـده عـبور میكنند. بر اساس انتخاب از پيش تعيين شده ، سلولهای مجزا كه بار خالص مثبت يا بار خالص منفی دارند به سمت مخزن جمع آوری مــربــوطــه مـنـحــرف شـده و بـقـيـه مـايـع و سلولها دور ريخته میشوند.
يک نوع ديگر فلوسيتومتر جدا كننده سلول يک مكانيزم مكانيكی برای جدا كردن دارد كه در آن لوله گيرنده سلول هايی كه خارج می شوند ، بـــه سـمـــت چـــپ و راســـت حـــركـــت كــرده و سلولهای موردنظر را می گيرد. اين نوع تكنولوژی مرتب سازی وابسته به تشكيل قطره نيست و در يک محيط بسته اتفاق میافتد و بنابراين تشكيل بخارات و ريسک آلودگی ناشی از نمونههای خطرناک بيو را كم میكند.
فلوسيتومترهای مدرن میتوانند چند هزار ذره را در هر ثانيه به صورت زمان حقيقی تحليـل كننـد و میتوانند به صورت فعال ، ذرات با ويژگی های خاص را جدا كنند. فلـوسيتومتر مشابه ميكروسكوپ است ، با اين تفاوت كه به جای توليد تصويری از سلول ، به صورت اتوماتيک پارامترهای مجموعه با خروجی بالا (برای تعداد زيادی سلول) را كمی میكند. برای آناليز بافتهای جامد ، بايد آنها را ابتدا در حالت محلول تک سلولی آماده كرد.
فلوسيتومتر پنج جزء اصلی دارد:
فلوسل: كه سلولها را در مايع هم راستا میكند ، به نحوی كه به صورت تک به تک پشت سر هم از مسير پرتو نوری عبور كنند.
سيستم اپتيكی و ليزر: كه معمولا از سيستمهای نوری و اندازه گيری امپدانس (يا هدايت) لامپها (جيوه ، زنون) ؛ ليزرهای با توان بالا و خنک شونده با آب (آرگون ، كريپتون ، ليزر رنگی) ؛ ليزرهای توان پائين خنک شونده با هوا (آرگون nm 488 ، هليم-نئون قرمز nm 633 ، هليم نئون سبز ، HeCd) UV)) ؛ ليزرهای ديودی (سبز ، قرمز ، بنفش و آبی) كه سيگنالهای نوری میدهند.
آشكارساز و سيستم تبديل آنالوگ به ديجيتال: كه FSC و SSC و نيز سيگنالهای فلـورسنـس نـور را بـه سيگنالهای الكتريكی (قابل پردازش توسط كامپيوتر) تبديل میكنند.
يک سيستم تقويت الكترونيكی: خطی يا لگاريتمی
يک كامپيوتر برای آناليز سيگنال ها
دريافت سيگنال سلولها
جمع آوری سيگنال از نمونهها با استفاده از فلوسيتومتر ، دريافت يا Acquisition ناميده میشود. دريافت ، به واسطه ی كامپيوتری كه به صورت فيزيكی به فلوسيتومتر متصل شده است و نرم افزاری كه واسطه ديجيتال با سيتومتر است ، انجام میشود. نرمافزار میتواند پارامترها (مانند ولتاژ ، جبرانسازی و غيره) را برای نمونه در حال تست تنظيم كند و همچنين برای اطمينان از اين كه پارامترها به صورت صحيح تنظيم شده اند ، می تواند در نمايش اطلاعات اوليه سلول همزمان با اخذ دادههای سلول كمک كند. بطور کلی فلوسيتومترهای اوليه ، دستگاههای تجربی بودند ؛ اما پيشرفتهای تكنولوژيک امكان اسـتفـاده وسيـع از آنهـا بـرای اهـداف بـالينـی و تحقيقاتی را فراهم كرده اند. به خاطر اين توسعه ، بازار قابل توجهی مربوط به ابزار دقيق ، نرم افزار آناليز و نيز معرفهای مورد استفـاده در مـرحلـه دريـافـت مـاننـد آنتی بادیهای برچسب گذاری شده به صورت فلورسنت ايجاد شده است.
دسـتـگـــاههـــای مــدرن مـعـمــولا چـنــد لـيـزر و آشكارساز فلورسنس دارند. ركورد فعلی برای يک دستگاه تجاری چهار ليزر و 18 آشكارساز فـلــورسـنــس اســت. افــزايــش تـعــداد لـيــزرهــا و آشـكــارســازهــا ، امكـان بـرچسـب گـذاری چنـد آنتیبادی به صورت همزمان را فراهم میكند و مـیتـوانـد با دقت بيشتری جمعيت هدف را با مـاركـرهــای فـنـوتـيـپ آنهـا شنـاسـايـی كـنـــد. دسـتـگـــاههــای خــاصــی حـتـی مـیتــوانـنــد از سلولهای مجزا هم تصاوير ديجيتال تهيه كنند و بــه ايــن وسـيـلــه امـكــان آنــالـيــز مـكــان سـيـگـنـال فـلــورسـنــت داخــل يــا روی سطـح سلـولهـا را میدهد.
آناليز داده
داده توليدشده با فلوسيتومترها را میتوان با رسم يک هيستوگرام يک بعدی نمايش داد يا اين كه به صورت دو يا حتی سه بعدی رسم كـرد. نـواحـی روی اين نمودارها را میتوان بر اساس شــــدت فــلــــورســنــــس ، بــــا ايــجــــاد يـــک ســـری زيرمجموعه به نام gate به صورت متوالی جــدا كـــرد. پــروتكـلهـای خـاصـی بـرای ايجـاد gateها برای اهداف بالينی و تشخيصی به ويژه در رابطه با هماتولوژی وجود دارند.
نمـودارهـا اغلـب بـا مقيـاس لگـاريتمـی رسـم میشوند. از آنجا كه طيفهای تابشی نورهای فـلـورسـنـت مـخـتـلـف بـا هـم هـمـپـوشـانی دارند ، سـيـگـنـالهـا در آشـكـارسـازهـا بـايـد بـه صورت الكترونيكی و نيز محاسباتی جبرانسازی شوند. داده جمع آوري شده با استفاده از فلوسيتومتر را مـــيتـــوان بـــا نـــرم افــزارهــايــی مــانـنــد WinMDI (يـک نرمافزار رايگان) ، Flowjo ، FCS Express ، VenturiOne ، CellQuest Pro يا Cytospec تحليل كرد. بعد از جمع آوری داده ، نيازی نيست كه اتـصال به فلوسيتومتر باقی بماند. به اين دليل ، آناليز معمولا روی يک كامپيوتر جداگانه انجام میشود.
آناليز محاسباتی
پيشـرفـتهـای اخيـر در شنـاسـايی اتوماتيک جـمـعـيـــت سـلـــولـــی مـــورد نـظــر بــا اسـتـفــاده از روشهای محاسباتی ، روش ديگری به عنوان جـايگـزيـن برای استراتژی سنتی gate پيشنهـاد مـــیكـنـنــد. سيستــمهـای شنـاسـايـی اتـومـاتيـک ، میتوانند به يافتن جمعيتهای پنهان و كمياب كمک كنند.
برچسبها
بـرچسـبهـای فلـورسنـت: بـازه وسيعـی از فلئـوروفـورهـا میتوانند به عنوان برچسب در فلوسيتومتری استفاده شوند. فلئوروفورها يا به صورت ساده "فلئورها" ، معمولا به يک آنتی بادی متصل میشوند كه يک ويژگی هدف را داخل يا روی سلول شناسايی میكند. همچنين میتوانند به يک ذره شيميايی كه ميل تركيبی با غشای سلول يا ساختار ديگری در سلول دارد ، متصل شوند. هر فلئوروفور ، يک طول موج تابش و پيک تحريک خاص دارد و طيفهای انتشار اغلب با هم همپوشاني دارند. در نتيجه تركيب برچسبهايی كه میتوانند استفاده شوند ، وابسته به طول موج لامپ (ها) يا لـيــزر(هــا)ی مــورد اسـتـفــاده بــرای بــرانـگـيـخـتــن فـلـئــوروكــورومهــا و نـيــز وابـستـه بـه آشكارسازهای موجود است. ماكزيمم تعداد برچسبهای فلورسنت قابل تفكيک حـدود 17 تـا 18 عـدد است و اين سطـح پيچيـدگـی بـاعـث مـیشـود نيـاز بـه بهينـه سـازی پـرزحـمتی برای محدودكردن اغـتـشــاشــات و نـيــز نـيــاز بــه الـگـوريتـمهـای deconvolution پيچيـده بـرای جـداسـازی طيفهايی كه با هم تداخل دارند ، باشد.
نقاط كوانتومی: نقاط كوانتومی به خاطر پيکهای انتشار باريک تر ، گاهی به جاي فلئوروفورهای سنتی استفاده میشوند.
برچسب گذاری ايزوتوپ: يک روش برای غلبه بر محدوديت برچسب گذاری فلورسنت ، متصل كردن ايزوتوپهای لانتانيدها (lanthanide) به آنتی بادیها است. اين روش از نظر تئوری میتواند امكان استفاده از 40 تا 60 برچسب قابل تمايز را فراهم كند و عملا كاربری آن ، برای 30 برچسب نشان داده شده است. سلولها وارد پلاسما شـده ، يـونـيـزه میشوند و اسپكترومتری جرمی برای شناسايی ايزوتوپهای مرتبط استفاده میشوند. گرچه اين روش امكان استفاده از تعداد بيشتری برچسب را فراهم میكند ، در حال حاضر ظرفيت عبوردهی كمتری نسبت به فلوسيتومتری سنتی دارد. همچنين سلولهای آناليزشده را از بين می برد و لذا امكان ريكاور كردن آنها با جدا سازی وجود ندارد.
پارامترهای اندازه گيری
در ادامه ليستی از اين پارامترها نوشته شده است كه البته دائماً اين ليست در حال توسعه است:
- تأييد تشخيص لوسمی لنفوسيتی مزمن
- پيچيدگی مورفولوژيک و حجم سلول ها
- رنگدانههاي سلول مانند كلروفيل يا phycoerythrin
- محتواي كلی DNA سيكل سلولی ، كينتيک سلولی ، تكثير ، پلوئيدی ، آنيوپلوئيدی و غيره)
- محتوای كلی RNA
- تغييرات تعداد كپی DNA (با تكنولوژی BACs-on-Beads يا Flow-FISH)
- مرتب سازی و آناليز كروموزوم (ايجاد كتابخانه ، رنگ كردن كروموزوم)
- بخش بندی و بيان پروتئين
- تغييرات پروتئين ، فسفوپروتئين ها
- مـحـصــولات تــراريـختـه (transgenic) در داخل بدن ، به ويژه پروتئين فلئورسنت سبز يا ديگر پروتئينهای فلئورسنت مرتبط
- آنتـی ژنهـای سطح سلول (خوشه ای از نشانگرهای افتراق (CD))
- آنــتـــــی ژنهـــــای درون ســلــــولــــی (انــــواع cytokines ، واسطههای ثانويه ، غيره.)
- آنتي ژنهای هسته ای
- فعاليت آنزيمی
- PH ، كـلـسـيـم يـونيـزه شـده داخـل سلـولـی ، منيزيم ، پتانسيل غشا
- سياليت غشا
- آپوپتوز (كمی سازی ، اندازه گيری تخريب DNA ، پـتـانـسـيـل غـشـای مـيـتـوكندری ، تغييرات نفوذپذيری ، فعاليت (caspase)
- زيست پذيری سلول
- مــانـيـتــور كــردن نـفــوذپـذيـری الـكـتـريـكـی سلولها
- بـــــررســـــی مـــشــخــصــــههــــای مــقــــاومــــت چنددارويی (MDR) در سلولهای سرطانی
- Glutathione
- تــــركــيــبــــات ويــــروســــی (آنــتــــی ژنهـــای سطح/DNA ، غيره.)
- چــســبــنــــدگـــی سـلـــول (بـــه عـنـــوان مـثـــال چسبندگی سلول پاتوژن-ميزبان)
كاربردها
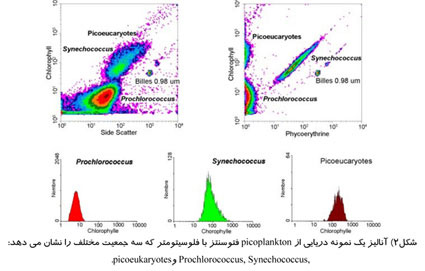
ايـن تـكـنـولـوژی كـاربـردهـايـی در زمينههای مـخـتـلـف شامل بيولوژی مولكولی ، پاتولوژی ، ايـمـنـولـوژی ، زيـسـت شـنـاسی گياهی و زيست شـنـاسـی دريـايـی دارد. كـاربـردهـای وسيعی در پـــزشــكـــی (بــه ويــژه در پـيــونــد ، هـمــاتــولــوژی ، ايـــمـــنـــــولــــوژی تــــومــــور و شــيــمــــی درمــــانــــی ، تـشـخـيـصهـای پـيـش از تولد ، ژنتيک و مرتب سازی اسپرم برای انتخاب جنسيت از قبل) دارد. در زيـسـت شـنـاسـی دريـايـی ، مـیتـوان خواص اتوفلورسنت پلانكتون فتوسنتز را با فلوسيتومتر به منظور توصيف ساختار اجتماعی و فراوانی اســتــخــــراج كــــرد. در مــهــنــــدســــی پـــروتــئــيـــن ، فلوسيتومتر در تركيب با نمايشگر باكتريائی و نـمــايـشـگــر مـخـمــر بـرای شنـاسـايـی گـونـههـای پـــروتـئـيـنــی cell surface-displayed بــا خــواص موردنظر استفاده میشود.
مشكلات گزارش شده
تحليل با استفاده از فلوسيتومتری نيازمند اين اسـت كـه سـلـولهـا به صورت مجزا در حالت محلول قرار داشته باشند (يعنی هر سلول به وسيله يک ماتريس مايع احاطه شده باشد ، بدون اين كه سلولهای همسايه در كنار آن جمع شده باشند.) خون ، مغز استخوان و كشتهای سلولی به راحتی ، محلولهای تک سلولی تشكيل میدهند. اما بافت جامد غيرلنفوئيد نياز به پردازش با استفاده از آنزيم يا عوامل (chelating) برای از بين بردن پيوندهای بين سلولها دارد. متأسفانه اين پردازش ، باقيماندههای سلولی (استرومای سلولی ، سيتو پلاسم و نوكلئوپلاسم آزاد) هم توليد میكند كه در طول تحليل ، اغتشاش ايجاد میكنند. با اين وجود میتوان با استفاده از تمايز و جبران الكترونيكی داده ها ، تأثير اين باقيماندهها روی نتايج نهائی را از بين برد.
برای اين كه فلوسيتومتر بتواند به صورت مؤثری كار كند ، نقطه تقاطع پرتو ليزر و جبران سلولی بايد در رابطه با مسير تشخيص ، دقيقاً حفظ شود. اين پيكربندی خاص نياز دارد كه عملكرد به صورت روزانه بررسی شود تا از عملكرد مناسب دستگاه ، اطمينان حاصل شود.

توصيههای خريد
توصيههای ECRI
با توجه به كاربردهای متنوع بالينی دستگاه فلوسيتومتر ، خريداران بايد نيازهای خود را ارزيابی كرده و دستگاه مناسب را بر اساس نيازهای خاص خود انتخاب كنند.
در حــالــت كـلــی ECRI تــوصـيــه مــیكـنــد كــه فـلــوسـيـتـومتـرهـا بـايـد قـادر بـه انجـام immunophenotyping باشند. قابليتهای ديگر (به عنوان مثال پيوند ، DNA S-phase و ميكروبيولوژی) اختياری هستند و بايد مطابق با نيازهای مكان خاصی كه قرار است دسـتـگـاه در آن اسـتـفـاده شـود ، در نـظـر گـرفـتـه شـونـد. نيازمندیهای طول موج برای فلوسيتومترها بر اساس تعداد رنگهای مورد استفاده در آناليز متفاوت است. زمانی كه با دو يا سه رنگ كار میشود ، طول موج nm 488 نياز است. زمانی كه با چهار يا شش رنگ كار می شود ، طول موج بالاتر نزديک به nm 560 يا nm 640 ترجيح داده میشود. ECRI تـوانـایی خـوانـدن دو تـا سـه رنـگ را بـه عنوان يک نيازمندي اصلی در نظر میگيرد. دستگاههايی كه میتوانند چهار رنگ را تشخيص دهند ، ترجيح داده میشوند و آناليز شش رنگ هم بايد اختياری در نظر گرفته شود.
ECRI توصيه میكند كه قابليت جدا سازی سلول به عنوان يک ويژگی اختياری در نظر گرفته شود. خريداران نياز دارند ارزيابی كنند كه آيا قابليت جدا سازی برای كار و نيازمندیهای خاص آنها الزامی است يا نه.
ملاحظات ديگر
از آنجا كه عملكرد فلوسيتومتر نياز به آموزش خــاص دارد ، تـوليـدكننـدگـان معمـولا آمـــوزش رايگـان ارائـه مـیدهنـد. بـا ايـن وجـود اپـــراتـــورهـــا بـــرای حـــرفـــه ای شـــدن ، نــيـــاز بـــه آمـوزشهـای اضـافـی و تجـربـه طـولانـی كار با دستگاه را دارند. بـه هـمـيـن دلـيـل در بـرخـی مـراكـز ، تـكـنـولـوژيـسـتهـای خـــاصـــی بـــرای كــار بــا فــلــــوســيـتـــومـتـــر در نـظـــر گـــرفـتـــه مـــیشـــونـــد. بيمارستانها همچنين بايد در اين زمينه كه نتايج چگونه مورد استفاده قرار خواهند گرفت و اين كـه چـه تستهايی بايد انجام شود ، با پزشكان ارتـبــاط داشـتــه بــاشـنــد. در هـنـگــام خــريـد يـک فلـوسيتـومتـر ، بـايد نيازمندیهای پرسنل را نيز مدنظر قرار داد (به عنوان مثال آيا نياز به استخدام يک پزشک يا تكنولوژيست باتجربه هست؟)
قيمت دستگاه بسته به سخت افزار و نرم افزار كــامـپـيــوتــر ، بـرنـامـههـای مـوجـود در دستگـاه و موجود بودن واحدهای آماده سازی اتوماتيک نمونه و ديگر لوازم جانبي متفاوت است. از آنجا كـه مـدلهـای بـا قـابـلـيـت جـدا سازی سلول و بدون آن موجود هستند ، آزمايشگاهها بايد تعيين كنند كه آيا به اين قابليت در حال حاضر نياز دارند يا ممكن است در آينده به آن نياز پيدا كنند. قيمت ايـن دسـتـگـاههـا بـسـتـه بـه گزينهها و پيكربندی دستگاه متغير است.
از آنـجـا كــه فـلـوسـيـتـومـتـرهـا ، دسـتـگـاههـای open-platform ای هستند ، معرفها را میتوان از تــولـيــدكـنـنــدگــان مـتـنــوعــی خــريــداری كــرد. معيارهای ديگری كه در خريد بايد در نظر گرفته شوند ، گزينههای مربوط به چاپگر و كامپيوتر ، گزينههای نرم افزار DNA و ايمنوفلورسانس و ويژگی هايی مانند محدودكردن خطرات بيو و سردسازی هستند.
در ادامه يک آناليز PV/LCC نمونه در آمريكا برای محاسبه هزينه تهيه يک فلوسيتومتر نوشته شده است:
فرضيات
- هزينههای عملكردی براي سالهای يک تا پنج در نظر گرفته میشوند.
- ضريب كاهش دلار %5/3 است.
- نرخ تورم برای هزينههای پشتيبانی 3% و برای مواد مصرفی 3% است.
هزينههای Capital
- سيستم: صد و چهل هزار دلار
- كل هزينههای Capital: صد و چهل هزار دلار
هزينههای عملكردی
- قرارداد سرويس ، دو تا پنج سال = چهارده هزار دلار در سال
- دستمزد و هزينهها براي يک FTE = چهل هزار دلار در سال
- معرفها = 105 هزار دلار در سال
- كل هزينههای عملكردی = 145 هزار دلار براي سال اول ؛ 159 هزار دلار برای سال دوم تا پنجم.
- $127‚805=PV
هزينههای ديگری كه در آناليز بالا وارد نشده اند و بايد برای برنامه ريزی بودجه در نظر گرفته شوند ، شامل موارد مرتبط با گزينههای زير میشوند:
- ارتقاء نرم افزار كه در گارانتی يا در قرارداد سرويس در نظر گرفته نشده اند.
Utilities -
- Contributions to overhead
همان طور كه در مثال بالا از آناليز PV/LCC نشان داده شد ، هزينه خريد اوليه فقط كـســری از هـزينـه كلـی عملكـرد در طـول پنـج سـال اسـت. بنـابـرايـن بـه جـای ايـن كـه تصميمگيری در مورد خريد تنها بر اساس هزينه اوليه يک سيستم فلوسيتومتر گرفته شود ، خريداران بايد هزينههای عملكردی در طول عمر آن را نيز در نظر گرفته و بررسی كنند.
مراحل توسعه
كـاربـردهـای بـالـيـنـی فـلـوسـيـتـومـتـر در اواسـط دهـه 1970 شـروع شـد. پيشرفت در سيستمهای الكترونيكی و افزوده شدن ميكروپروسسورها به فلوسيتومترهای فعلی امكان ارزيابی حداقل هشت تا نه پارامتر سلولی را میدهد ؛ دو پارامتر پراكندگی نور ، سه يا چهار پارامتر chromogenic و سه پارامتر ايمنوفلورسانس.
به علاوه امروزه بسياری از فلوسيتومترها ، مجهز به دو يا چند ليزر هستند كه میتوانند بـرای بـرانـگـيـختن يک بازه از رنگها و فلئوروكرومها استفاده شوند. اين پيشرفت تكنولوژی برای اپراتورها امكان استفاده همزمان از 11 رنگ ايمنوفلورسانس را فراهم میكند.
به منظور بهبود دادن كلاس بندی ، دريافت و آناليز داده ، نرم افزار آناليز داده به طور دائم به روز شده و توسعه داده میشود. به علاوه استفاده از سيستمهای آماده سازی اتـومـاتيک نمونه ، موجب استانداردسازی آماده سازی و فراهم كردن كنترل كيفيت خوب میشود و زمان آماده سازی را از يک تا دو ساعت به 10 دقيقه يا كمتر كاهش مـیدهـد. محققـان نشان دادهاند كه تكنولوژی فلوسيتومتر با استفاده از منابع نوری ارزان قيمت هــلــيــــم-نــئـــون و تـكـنـيـــک هـــای رنـــگ آمـيـــزی فـلـورسـانـس میتوانند ابزاری حساس ، از نظر هزينه مقرون به صرفه و سريع برای تشخيص ، توصيف و شناسايی باكتری ها باشند. امروزه ، يــكـــی از مـــرســوم تــريــن كــاربــردهــای بــالـيـنــی فلوسيتومتر انجام شمارش لنفوسيت 8/CD4CD در خــون محيطـی از بيمـاران بـا HIV مثبت برای سـطــح بـنــدی و بـرای نـظـارت دوره ای اســت. تـحـقيقـاتـی بـا هـدف مطـالعـه پلاكتها به ويـژه بــــرای تــشــخــيـــص آنــتـــی بـــادی ضـــدپـــلاكــتــی مـــرتــبـــط بــا بـيـمــاری هــای خــود ايـمـنــی انـجــام مـیشـونـد. يـكـی ديـگـر از زمينههای تحقيقاتی مورد علاقه ، فعال سازی پلاكت است كه زمانی كه خون با پروتز رگ يا سطح يک وسيله پزشكی مـانـنـد واحـد هـمودياليز يا بای پس شش-قلب تـمـاس پـيدا می كند ، اتفاق میافتد. آناليز DNA سـلــول تــومـور و نـيـز بـسـيـاری از كـاربـردهـای ميكروبيولوژی بالينی ديگر برای فلوسيتومتر با افزايش مداوم استفاده از اين دستگاه ، در حال بررسی است.
محققـان شـروع به بررسی امكان استفاده از فلوسيتومترها به عنوان آشكارسازهای ويروس كـــرده انـــد. ويـــروسهــا بـسـيــار كــوچــکتــر از بـاكتریها يا سلولهای سرطانی با قطر 100 تا 250 نــانــومـتــر هـسـتـنــد. انـدازه كـوچـک آن هـا ، تفكيک كردن سيگنالهای نور پراكنده شده از آنهـا از نـويـز پـس زمـيـنـه را مـشـكـل مـیسازد. هـــمزمـــان بـــا تـــلاش مــحـقـقــان بــرای افــزايــش حساسيت فلوسيتومترها ، نقش اين دستگاهها به عنوان آشكارساز ويروس پررنگ تر میشود.
منبع: ماهنامه مهندسی پزشکی
نظرات شما عزیزان:

